新闻消息
【通知公告】临床研究招募丨晚期骨肉瘤患者新治疗选择:多中心Ⅲ期研究正式启动
尊敬的患者及家属:
中国医学科学院肿瘤医院山西医院(山西省肿瘤医院)骨软组织肿瘤科正在开展一项注射用 HS-20093 对比吉西他滨联合多西他赛治疗既往二线治疗失败骨肉瘤患者的多中心Ⅲ期临床研究(ARTEMIS-011)。本研究已通过我院伦理委员会审批(批件号:YW2025032),旨在为晚期骨肉瘤患者探索更有效的治疗方案,现面向全国招募符合条件的受试者。
一、研究背景:聚焦晚期治疗难题
骨肉瘤是最常见的骨原发恶性肿瘤,好发于20岁以下儿童及青少年,以长骨干骺端为多发部位。尽管手术切除联合新辅助化疗显著提升了早期患者的保肢率与生存期,但晚期及转移性病例仍面临治疗手段有限的挑战。近年来,靶向治疗与免疫治疗的发展为该领域带来突破希望,本次研究正是针对二线治疗失败的患者群体,将创新药物与传统化疗方案进行对比,探索更有效的后续治疗方案。
二、项目名称
评估注射用HS-20093对比吉西他滨联合多西他赛治疗既往二线治疗失败的骨肉瘤有效性和安全性的随机、对照、开放、多中心Ⅲ期临床研究(ARTEMIS-011)
三、招募标准
注:研究参与者必须符合以下所有标准
研究参与者需≥12周岁,经至少二线治疗后进展或不耐受的骨肉瘤患者
·年龄与病理:≥12 周岁,经病理学确诊为骨肉瘤(需提供明确诊断所需关键性免疫组化/肿瘤细胞表型结果),且已接受至少 3 种标准一线治疗药物(甲氨蝶呤、蒽环类药物、顺铂、异环磷酰胺中任选 3 种及以上)治疗。
·病灶要求:根据 RECIST 1.1 标准存在可测量靶病灶(未经过照射等局部治疗的、或经局部治疗后明确进展的可测量病灶。排除仅有骨或脑病灶作为靶病灶)。
·体能状态:美国东部肿瘤协作组(ECOG)体力状况评分(PS) 为0-1 分,且近 2 周内无恶化,最小预期生存期≥12 周。
·避孕要求:有生育能力的研究参与者从签署知情同意起到末次给药或终止治疗(以晚发生者为准)后 6 个月内采取有效避孕措施(女性禁止哺乳)。
四、参与权益与获益
·专业医疗评估:免费接受研究相关检查(如影像学、血液学检测)及专家诊疗指导;
·创新治疗机会:随机分配至创新药物组或传统化疗组,均由经验丰富的医疗团队全程管理;
·患者支持服务:研究期间交通补贴、心理支持及病情跟踪随访。
五、如何参与?
1.咨询方式:
联系电话:0351-4651265/0351-4651412 (工作日 8:30-18:00)联系人:张俊杰、付明芳、齐环宇
现场咨询:5号楼21层骨软组织肿瘤病区或门诊咨询
2. 门诊时间(2025年5月)
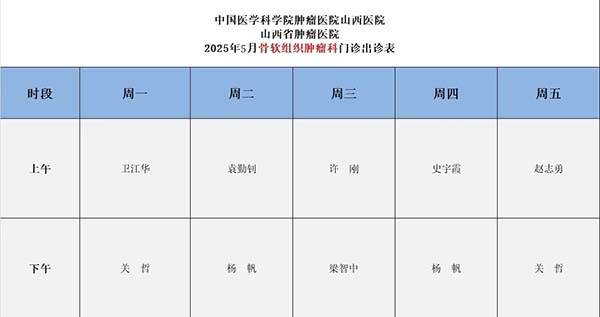
3. 报名流程
初步沟通→提交病历资料→医学评估→签署知情同意书→入组治疗
六、研究信息
· 牵头科室:骨软组织肿瘤科
· 研究期限:即日起至满额为止
· 伦理声明:研究遵循《赫尔辛基宣言》及国家临床试验规范,患者权益受独立伦理委员会全程监督。
如果您或您的家属符合上述条件,欢迎联系我们了解详情。参与临床研究可能为晚期治疗带来新的希望,我们将以专业团队为您提供全程支持。
中国医学科学院肿瘤医院山西医院
山西省肿瘤医院 骨软组织肿瘤科
2025年5月
医院地址
院本部:山西省太原市杏花岭区职工新村3号
南院区(乳腺诊疗中心):山西省太原市小店区创新街3号





 晋公网安备14010702074528
晋公网安备14010702074528